
Mol, basınç birimi olarak kullanılır mı?
Bu yazıda, molün basınç birimi olarak kullanımıyla ilgili yanlış anlamalara ve kavram karışıklıklarına dikkat çekilmektedir. Mol, kimyada bir miktar birimi olarak önemli bir role sahipken, basınç birimi olarak kabul edilmediği vurgulanmaktadır. Ayrıca, ideal gaz yasası gibi kavramlarla molün basınçla ilişkisi açıklanmaktadır.
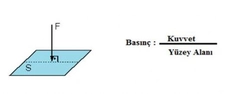
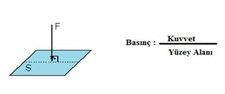
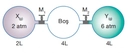
Mol, Basınç Birimi Olarak Kullanılır mı?Mol, kimyada kullanılan temel birimlerden biridir ve miktar birimi olarak tanımlanır. Ancak, basınç birimi olarak kullanılması, bazı yanlış anlamalara ve kavram karışıklıklarına yol açabilir. Bu makalede molün, basınç birimi olarak kullanımına dair detaylar ele alınacaktır. Mol Nedir?Mol, bir maddenin miktarını ifade eden bir birimdir ve Avogadro sayısı (yaklaşık 6.022 x 10²³) kadar parçacık içerir. Bu parçacıklar atom, molekül, iyon veya başka bir türde olabilir. Mol, SI birim sisteminin temel birimlerinden biri olup, maddelerin miktarını ölçmek için yaygın olarak kullanılır. Basınç Nedir?Basınç, bir yüzeye uygulanan kuvvetin, o yüzeyin alanına bölünmesi ile hesaplanan bir fiziksel büyüklüktür. SI birim sisteminde basınç birimi Pascal (Pa) olarak tanımlanır. 1 Pascal, 1 Newton'lık kuvvetin 1 metrekarelik alana uygulanmasıyla oluşan basıncı ifade eder. Mol ve Basınç İlişkisi Mol, doğrudan bir basınç birimi değil, ancak gazların davranışını anlamada önemli bir yere sahiptir. Ideal gaz yasası, bir gazın basıncını, sıcaklığını, hacmini ve mol sayısını bir araya getirir. Bu yasa şu şekilde ifade edilir:\[ PV = nRT \]Burada;- \( P \): Basınç (Pa)- \( V \): Hacim (m³)- \( n \): Mol sayısı (mol)- \( R \): Gaz sabiti (8.314 J/(mol·K))- \( T \): Sıcaklık (K) Bu denklemde mol sayısı, gazın basıncı ile ilişkili olan bir faktördür. Ancak mol, basınç birimi olarak kullanılmaz. Molün Basınç Birimi Olarak Yanlış Kullanımı Molün basınç birimi olarak kullanılması, bilimsel iletişimde yanıltıcı olabilir. Bazı durumlarda, özellikle laboratuvar ortamlarında, mol sayısının basıncı etkileyen bir faktör olduğunu belirtmek için dolaylı bir şekilde ifade edilebilir. Ancak, bu durum, molün bir basınç birimi olduğu anlamına gelmez. Sonuç Mol, miktar birimi olarak önemli bir rol oynamasına rağmen, basınç birimi olarak kullanılmaz. Basınç ölçümleri için Pascal, bar, atmosfer gibi birimler tercih edilir. Mol, gazların davranışını anlamak için gerekli bir ölçü birimi olsa da, doğrudan bir basınç birimi değildir. Ekstra Bilgiler Bu makale, molün basınç birimi olarak kullanılmaması gerektiğini vurgulamakta ve bu konudaki yanlış anlamaları ortadan kaldırmayı amaçlamaktadır. |


















Molün basınç birimi olarak kullanılıp kullanılmadığı hakkında düşündüğümde, kimyada molün önemli bir miktar birimi olduğunu biliyorum. Ancak, basınç birimi olarak kullanılmasının yanlış anlaşılmalara yol açabileceğini de anlıyorum. Mesela, ideal gaz yasası çerçevesinde mol sayısının basınçla ilişkili olduğunu görmek mümkün, ama bu durum molün doğrudan bir basınç birimi olduğu anlamına gelmiyor. Sizce de laboratuvar ortamlarında bu tür kavram kargaşalarının önüne geçmek için net tanımlar yapılması gerekli değil mi?
Sanay,
Molün Kullanımı
Mol, kimyada önemli bir miktar birimi olarak kabul edilmektedir. Ancak, basınç birimi olarak kullanılması gerçekten de bazı karışıklıklara yol açabilir. Basınç, genellikle pascal (Pa) veya atmosfer (atm) gibi birimlerle ifade edilirken, mol sayısı gazların davranışını anlamada kritik bir rol oynamaktadır.
İdeal Gaz Yasası
İdeal gaz yasası çerçevesinde mol sayısının basınçla ilişkisi doğru bir şekilde tanımlanabilir. Ancak, burada dikkat edilmesi gereken nokta, molün bir basınç birimi olmadığıdır. Bu tür yanlış anlamaların önüne geçmek adına, kavramların net bir şekilde tanımlanması son derece önemlidir.
Laboratuvar Ortamları
Laboratuvar ortamlarında bu tür kavram kargaşalarının önüne geçmek için, eğitim materyallerinin ve uygulamaların daha dikkatli bir şekilde hazırlanması gerekmektedir. Net ve anlaşılır tanımlar, hem öğrencilerin hem de profesyonellerin konuyu daha iyi kavramalarına yardımcı olacaktır. Bu sayede, kimya alanındaki çalışmalar daha sağlıklı bir zeminde ilerleyebilir.
Sonuç olarak, kavramların net tanımları, bilimsel iletişimi kolaylaştırır ve yanlış anlamaların önüne geçer. Bu noktada sizin görüşlerinize de katılıyorum.