
Basınç Hacim İlişkisi
Basınç ve hacim arasındaki ilişki, gazların davranışını anlamak için kritik bir temel sunar. Boyle ve Charles yasaları gibi temel kavramlar, bu ilişkiyi matematiksel olarak ifade eder. Termodinamik ilkeleriyle desteklenen bu bilgiler, mühendislik uygulamalarında verimliliği artırmak için hayati önem taşır.
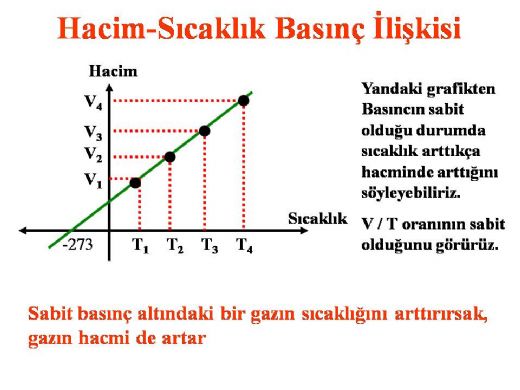
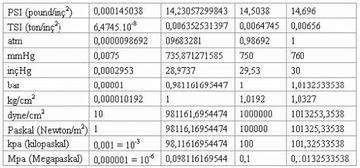
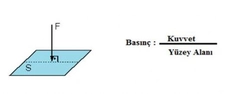
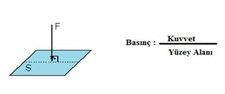
Basınç Hacim İlişkisi Basınç ve hacim arasındaki ilişki, fizik ve mühendislik alanlarında önemli bir yere sahiptir. Bu ilişki, gazların davranışını ve çeşitli sistemlerdeki akış dinamiklerini anlamak için kritik bir temel sunar. Özellikle termodinamik, akışkanlar mekaniği ve mühendislik uygulamalarında bu kavramların anlaşılması, enerji verimliliği ve sistem tasarımı açısından büyük önem taşır. 1. Temel Kavramlar Basınç, birim alana düşen kuvvet olarak tanımlanır ve genellikle Pascal (Pa) ya da atmosfer (atm) cinsinden ölçülür. Hacim ise, bir cismin kapladığı alanı ifade eder ve genellikle litre (L) ya da metreküp (m³) cinsinden ifade edilir. Bu iki kavram arasındaki ilişki, genellikle Boyle Yasası ve Charles Yasası gibi gaz yasaları ile açıklanır.
2. Gazların Davranışı ve Uygulamaları Gazların basınç ve hacim ilişkisi, birçok mühendislik uygulamasında kritik bir rol oynamaktadır. Özellikle içten yanmalı motorlar, kompresörler ve HVAC sistemleri gibi mekanizmalarda bu ilişki dikkate alınmaktadır.
3. Termodinamiğin Rolü Termodinamik, basınç ve hacim ilişkisini anlamak için temel bir bilim dalıdır. Birçok termodinamik süreçte, gazların basınç ve hacim değişimleri, sistemin enerji dengesini belirler. Termodinamik yasaları, bu ilişkilerin matematiksel modellerle açıklanmasına olanak tanır.
Sonuç Basınç ve hacim arasındaki ilişki, gazların fiziksel özelliklerini ve mühendislik uygulamalarını anlamak için temel bir kavramdır. Boyle ve Charles yasaları gibi temel gaz yasaları, bu ilişkilerin matematiksel olarak ifade edilmesine olanak tanırken, termodinamik ilkeler de bu süreçlerin arka planını açıklar. Gazların bu özellikleri, birçok endüstriyel uygulamada dikkate alınarak, sistemlerin verimliliğini artırmak ve enerji tasarrufu sağlamak için kullanılmaktadır. Bu nedenle, basınç hacim ilişkisi, hem akademik hem de pratik alanlarda önemli bir konu olarak karşımıza çıkmaktadır. Gazların davranışlarını anlamak, mühendislik tasarımlarında daha etkili ve verimli sistemlerin geliştirilmesine katkıda bulunur. |


















Boyle Kanunu'nun gazların davranışlarını açıklamadaki önemi nedir? Gazların basınç ve hacim değişikliklerine nasıl tepki verdiğini anlamak neden önemlidir? Özellikle dalgıçlar ve uçak mühendisleri için bu bilginin pratik kullanımları nelerdir? Boyle Kanunu'nun sadece ideal gazlar için geçerli olduğu belirtilmiş; gerçek gazların davranışlarını doğru bir şekilde anlamak için hangi modeller kullanılır? Van der Waals denklemi bu konuda nasıl bir fark yaratır?
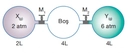
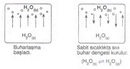
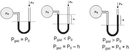
İlyas, Boyle Kanunu, gazların davranışlarını açıklamada önemli bir yere sahiptir. Bu kanun, sabit sıcaklıkta bir gazın hacmi ile basıncının ters orantılı olduğunu ifade eder. Yani, hacim azalırsa basınç artar ve tersi de geçerlidir. Gazların basınç ve hacim değişikliklerine nasıl tepki verdiğini anlamak, birçok pratik uygulamada kritik önem taşır.
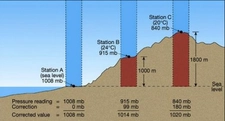
Dalgıçlar için bu bilgi, derinlik değişiklikleriyle birlikte basıncın artması veya azalması durumunda vücutlarındaki gazların hacimlerinin nasıl değişeceğini anlamaları açısından hayati önem taşır. Aynı şekilde, uçak mühendisleri de yüksek irtifalarda atmosferik basıncın değişmesiyle birlikte uçağın iç basıncını düzenlemek zorundadırlar.
Boyle Kanunu'nun sadece ideal gazlar için geçerli olduğu doğrudur. Gerçek gazların davranışlarını daha doğru anlamak için Van der Waals denklemi gibi daha karmaşık modeller kullanılır. Van der Waals denklemi, moleküller arasındaki etkileşimleri ve moleküllerin hacimlerini dikkate alarak, gazların gerçek davranışlarını daha gerçekçi bir şekilde açıklar. Bu da özellikle çok yüksek basınçlar veya çok düşük sıcaklıklarda gazların davranışlarını anlamada büyük fark yaratır.