
Kısmi basıncı toplam basınçla nasıl bulabilirim?
Kısmi basınç ve toplam basınç arasındaki ilişki, gaz ve sıvıların davranışlarını anlamada kritik bir rol oynar. Kısmi basınç, belirli bir molekülün toplam basınç içindeki etkisini ifade ederken, toplam basınç tüm moleküllerin oluşturduğu basıncı temsil eder. Dalton'un yasaları ile bu kavramlar birbirleriyle ilişkilendirilir.
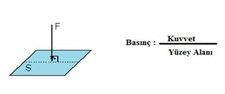
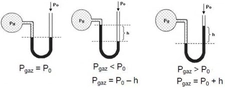
Kısmı Basıncı ve Toplam Basınç Arasındaki İlişki Kısmı basıncı, belirli bir gaz veya sıvı molekülünün, toplam basınç içindeki katkısını ifade eden bir terimdir. Bu kavram, gazların ve sıvıların davranışını anlamak için önemlidir. Toplam basınç ise, sistemdeki tüm gaz veya sıvı moleküllerinin oluşturduğu basıncı ifade eder. Kısmı basıncı, Dalton'un Kısmi Basınçlar Yasası'na dayanmaktadır ve bu yasa, bir gaz karışımındaki her bir gazın, toplam basınç üzerindeki etkisini açıklamaktadır. Kısmı Basıncın Hesaplanması Kısmı basıncı hesaplamak için aşağıdaki formül kullanılabilir:
Bu formül, ideal gaz yasası çerçevesinde kullanılmakta olup, gazların belirli koşullar altında nasıl davrandığını gösterir. Yukarıdaki formülde, kısmi basıncı bulmak için gazın mol sayısı, sıcaklık ve hacim gibi parametreler gereklidir. Toplam Basıncın Hesaplanması Toplam basıncı hesaplamak için, bir sistemde bulunan tüm gazların kısmi basınçlarının toplamı alınmalıdır:
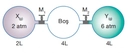
Bu formül, Dalton'un Kısmi Basınçlar Yasası'nın bir sonucudur ve toplam basıncın, her bir gazın kısmi basınçlarının toplamına eşit olduğunu belirtir. Kısmı Basıncı Hesaplamak için Örnek Bir gaz karışımında, A gazı, 2 mol, B gazı ise 3 mol olsun. Bu karışımın toplam basıncı 5 atm olarak verilmişse, her bir gazın kısmi basıncını aşağıdaki gibi hesaplayabiliriz: 1. Öncelikle, her bir gazın mol sayısını toplam mol sayısına oranlayarak kısmi basınçlarını bulalım. - Toplam mol sayısı = 2 + 3 = 5 mol - A gazının kısmi basıncı: P_A = (n_A / n_total) P_total = (2 / 5) 5 atm = 2 atm - B gazının kısmi basıncı: P_B = (n_B / n_total) P_total = (3 / 5) 5 atm = 3 atm Sonuç Kısmı basıncı, gazların ve sıvıların karışımlarında önemli bir kavramdır. Dalton'un Kısmi Basınçlar Yasası, kısmi basınçların hesaplanmasında temel bir ilkedir. İdeal gaz yasası ile birlikte kullanıldığında, gazların davranışlarını anlamak için kritik bir araçtır. Bu bilgiler, mühendislik, kimya ve fizik alanlarında geniş bir uygulama yelpazesine sahiptir. Ek Bilgiler Bu bilgiler, kısmı basıncı ve toplam basıncı anlamak için temel bir çerçeve sunmaktadır. Kısmı basıncı hesaplamak için gerekli olan temel yöntemleri ve örnekleri inceleyerek, bu kavramın pratikte nasıl uygulandığını öğrenmek mümkündür. |


















Kısmı basıncı ve toplam basınç arasındaki ilişkiyi öğrendiğimde, gazların ve sıvıların davranışlarını daha iyi anlamaya başladım. Dalton'un Kısmı Basınçlar Yasası'nın nasıl çalıştığını ve özellikle bir gaz karışımındaki her bir gazın toplam basınç üzerindeki etkisini kavramak oldukça önemli. Kısmı basıncın hesaplanmasında kullanılan formül, gazların mol sayısı, sıcaklık ve hacim gibi parametreleri dikkate alarak nasıl bir sonuç verdiğini görmek gerçekten ilginç. Örneğin, bir gaz karışımındaki farklı gazların kısmi basınçlarını hesaplayarak, aslında sistemin genel davranışını nasıl belirleyebileceğimizi anlamak beni etkiledi. Gerçek gazların ideal gaz yasasından sapmalar gösterdiğini öğrendiğimde ise, bu konuya daha fazla derinlik katacak olan Van der Waals denklemi gibi düzeltilmiş formüllerin de var olduğunu görmek faydalı oldu. Bu bilgilerin mühendislik ve çevresel bilimlerdeki uygulamaları, konunun ne kadar kapsamlı olduğunu gösteriyor. Bu konuda daha fazla bilgi edinmek ve pratikte uygulamalarını görmek beni heyecanlandırıyor. Sizce bu kavramları anlamak, özellikle mühendislik projelerinde ne kadar kritik bir öneme sahip?
Kısmı Basınç ve Toplam Basınç
Tatu, kısmi basınç ve toplam basınç arasındaki ilişkiyi anlamanın gazlar ve sıvılar üzerindeki etkilerini kavrayabilmek adına son derece önemli olduğunu belirtmişsin. Dalton'un Kısmi Basınçlar Yasası'nın gaz karışımlarındaki uygulamaları, mühendislik ve çevresel bilimler açısından kritik bir yer tutuyor. Bu yasayı ve gazların davranışlarını öğrenmek, sistemlerin genel davranışını anlamamıza yardımcı olurken, pratikteki uygulamaları da daha iyi değerlendirmemizi sağlıyor.
Gerçek Gazlar ve İdeal Gaz Yasası
Gerçek gazların ideal gaz yasasından sapmalarını gözlemlemek, özellikle mühendislik uygulamalarında büyük bir etkiye sahip. Van der Waals denklemi gibi düzeltilmiş formüller, gazların gerçek davranışlarını daha iyi yansıtıyor ve bu sayede mühendislik projelerinde daha güvenilir sonuçlar elde ediliyor.
Mühendislik Projelerinde Önemi
Bu kavramların mühendislik projelerinde kritik öneme sahip olmasının sebebi, sistemlerin tasarımında ve optimizasyonunda doğru hesaplamaların yapılması gerekliliğidir. Gaz ve sıvı dinamiği, reaktör tasarımları, enerji üretimi ve çevresel etki değerlendirmeleri gibi birçok alanda bu bilgilerin kullanılması, projelerin başarısını etkileyebiliyor.
Sonuç olarak, bu konulara olan ilgin ve derinlemesine bilgi edinme isteğin, mühendislik alanında sağlam bir temel oluşturmanı sağlayacaktır. Bu bilgileri pratikte uygulamak, hem kariyerin hem de projelerin açısından büyük bir avantaj sunacaktır.