
Basınç hacim yasası nedir ve nasıl çalışır?
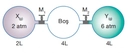
Basınç hacim yasası, gazların basıncı ile hacmi arasındaki ters ilişkiyi tanımlar. Hacim arttıkça basınç azalırken, hacim azaldıkça basınç artar. Bu yasa, gazların ideal koşullardaki davranışını anlamak için kritik öneme sahiptir ve mühendislik ile bilimsel uygulamalarda yaygın olarak kullanılır.
Basınç Hacim Yasası Nedir ve Nasıl Çalışır?Basınç hacim yasası, gazların davranışını anlamak için önemli bir fiziksel ilkedir. Bu yasa, gazların hacmi ile basıncı arasında ters bir ilişki olduğunu ifade eder. Yani, bir gazın hacmi artırıldığında, basıncı azalır; hacmi azaltıldığında ise basıncı artar. Bu ilişki, özellikle gazların ideal davranış gösterdiği koşullarda geçerlidir. Basınç Hacim Yasasının Temelleri Basınç hacim yasası, ideal gaz yasası ile doğrudan ilişkilidir. Ideal gaz yasası, bir gazın basıncı (P), hacmi (V) ve sıcaklığı (T) arasındaki ilişkiyi tanımlar. Bu ilişki şu şekilde ifade edilir:
Burada, n gazın mol sayısını, R gaz sabitini ve T ise Kelvin cinsinden sıcaklığı temsil eder. Basınç hacim yasası, sabit sıcaklık koşullarında (izotermal) gazın hacmi ile basıncı arasındaki ilişkiyi daha da detaylandırır. Basınç Hacim Yasası ve Boyle Yasası Basınç hacim yasası, özellikle Boyle Yasası ile de ilişkilidir. Boyle Yasası, sıcaklık sabitken (izotermal koşullar altında) bir gazın basıncı ile hacmi arasındaki ilişkiyi tanımlar. Boyle Yasası'na göre:
Burada P1 ve V1, gazın başlangıç basıncı ve hacmi; P2 ve V2 ise gazın son basıncı ve hacmidir. Bu formül, gazın hacmi arttıkça basıncının azaldığını veya hacmi azaldıkça basıncının arttığını gösterir. Gazların Davranışını Etkileyen Faktörler Basınç hacim yasası, gazların davranışını etkileyen birçok faktörü içerir. Bu faktörlerden bazıları şunlardır:
Uygulama Alanları Basınç hacim yasası, mühendislik, kimya ve fizik alanlarında geniş uygulama alanlarına sahiptir. Örneğin:
Sonuç Basınç hacim yasası, gazların davranışını anlamak için kritik bir öneme sahiptir. Bu yasa sayesinde, mühendislik uygulamaları ve bilimsel araştırmalar, gazların özelliklerini ve davranışlarını daha iyi anlayarak bu bilgilere dayalı yenilikçi çözümler geliştirebilmektedir. Bu yasa, gazların fiziksel özelliklerini belirleyen temel ilkelerden biridir ve bilimsel çalışmalarda sıklıkla kullanılır. |


















Basınç hacim yasası gerçekten de gazların davranışını anlamak için önemli bir kavram. Özellikle gazların hacimlerinin arttığında basınçlarının neden azaldığını merak ediyorum. Bu durum, gaz moleküllerinin birbirleriyle çarpışma sıklığını nasıl etkiliyor? Ayrıca, Boyle yasası ile olan ilişkisi de oldukça dikkat çekici. Hacim değişikliklerinin basıncı nasıl etkilediğine dair örnekler vermek bu konsepti daha iyi anlamama yardımcı olabilir mi? Gazların davranışını etkileyen faktörler arasında sıcaklığın rolü de önemli görünüyor. Sıcaklık arttığında moleküllerin kinetik enerjisinin nasıl değiştiğini ve bunun basıncı nasıl etkilediğini daha detaylı öğrenmek isterim. Uygulama alanları da oldukça geniş. Özellikle motor tasarımlarında bu yasanın nasıl uygulandığına dair daha fazla bilgi edinmek beni çok ilgilendiriyor.
Sayın Atasan bey, basınç-hacim ilişkisi ve gazların davranışına dair sorularınızı cevaplamaya çalışayım:
Hacim Artışı ve Basınç Azalması
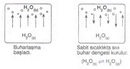
Gazların hacmi arttığında, aynı sayıda molekül daha geniş bir alana yayılır. Bu durumda moleküllerin kabın çeperleriyle çarpışma sıklığı azalır, dolayısıyla basınç düşer. Örneğin, bir şırınganın pistonunu çektiğinizde içerideki gazın hacmi artar ve basıncı azalır.
Boyle Yasası İlişkisi
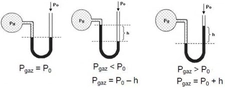
Boyle yasası tam olarak bu ilişkiyi tanımlar: Sabit sıcaklıkta, bir gazın basıncı ile hacmi ters orantılıdır (P₁V₁ = P₂V₂). Hacim iki katına çıkarsa, basınç yarıya iner.
Sıcaklığın Rolü
Sıcaklık arttığında gaz moleküllerinin kinetik enerjisi artar, daha hızlı hareket ederler ve kabın çeperleriyle daha sık ve şiddetli çarpışırlar. Bu da basıncın artmasına neden olur. Sabit hacimde, sıcaklık artışı doğrudan basınç artışına yol açar.
Motor Tasarımlarında Uygulama
İçten yanmalı motorlarda, piston silindir içinde hareket ederek hacmi değiştirir. Sıkıştırma stroğunda hacim azalır, basınç artar ve yakıt-hava karışımı sıkışır. Yanma sonucu oluşan yüksek basınçlı gazlar genleşerek pistonu iter ve mekanik iş elde edilir. Bu prensip, Boyle yasası ve gaz kanunları temelinde çalışır.
Bu konuları daha iyi anlamak için basit deneyler gözlemleyebilir veya interaktif simülasyonlar kullanabilirsiniz.