Sıcaklık ve basınç nasıl birbirini etkiler?
Sıcaklık ve basınç arasındaki ilişki, fiziksel bilimlerin temel taşlarından biridir. Bu ilişki, gazların davranışını anlamada ve endüstriyel süreçlerin yönetiminde kritik bir rol oynar. Sıcaklık artışı, gaz moleküllerinin kinetik enerjisini artırırken, basıncı da yükseltir. Bu kavramların etkileri, iklim biliminden mühendisliğe kadar geniş bir yelpazede uygulanmaktadır.
Sıcaklık ve Basınç İlişkisi Sıcaklık ve basınç, fiziksel bilimlerin temel kavramları arasında yer almakta olup, birçok doğal olayın ve endüstriyel süreçlerin anlaşılması açısından kritik öneme sahiptir. Bu iki kavram arasındaki ilişki, gazların davranışını anlamada ve çeşitli mühendislik uygulamalarında büyük rol oynamaktadır. Gazların Davranışı ve Temel Yasalar Gazların sıcaklık ve basınç ilişkisi, ideal gaz yasası ile açıklanabilir. İdeal gaz yasası, bir gazın sıcaklığı, basıncı ve hacmi arasındaki ilişkiyi tanımlayan bir denklemdir:
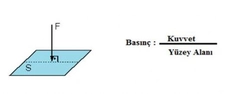
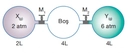
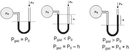
Burada;- P: Basınç,- V: Hacim,- n: Mol sayısı,- R: Gaz sabiti,- T: Sıcaklık. Bu denkleme göre, sıcaklık arttıkça basıncın da artması beklenir, eğer hacim sabit tutulursa. Buna "Gay-Lussac Yasası" da denir. Tersine, hacim sabitken sıcaklık düştüğünde basıncın da düşmesi gözlemlenir. Sıcaklık ve Basınç Arasındaki Bağlantılar Sıcaklık ve basınç arasındaki ilişki, gazların farklı durumlarda nasıl davrandığını anlamak için önemlidir. Örneğin:
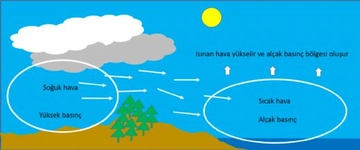
Bu ilişkiler, birçok fiziksel olaya, örneğin hava durumuna, iklim değişikliğine ve endüstriyel proseslere etki eder. Uygulama Alanları Sıcaklık ve basınç arasındaki etkileşimin uygulama alanları geniştir. Örneğin:
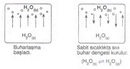
Ekstra Bilgiler Sıcaklık ve basınç arasındaki ilişki, gazların dışında sıvılar ve katılar için de geçerlidir. Örneğin, suyun kaynama noktası, atmosfer basıncına bağlı olarak değişir. Düşük basınç altında su daha düşük sıcaklıklarda kaynar. Bu durum, yüksek irtifalarda yemek pişirme sürelerini etkileyebilir.Ayrıca, sıcaklık ve basınç arasındaki ilişki, mühendislik uygulamalarında termodinamik döngülerin analizi ve enerji üretimi için kritik bir rol oynamaktadır. Sonuç Sıcaklık ve basınç arasındaki etkileşim, bilimsel ve mühendislik alanlarında önemli bir konudur. Bu iki kavramın birbirini nasıl etkilediğini anlamak, birçok doğal ve endüstriyel sürecin daha iyi anlaşılmasına ve yönetilmesine yardımcı olmaktadır. Gazların, sıvıların ve katıların davranışlarını etkileyen bu temel ilişkiler, hem teorik hem de pratik açıdan büyük bir öneme sahiptir. |