
Kimyada basınç birimleri nelerdir ve nasıl kullanılır?
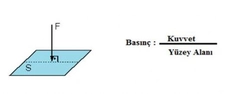
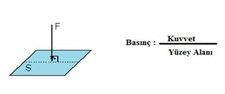
Kimyada basınç, birim alana uygulanan kuvvet olarak tanımlanır ve gazların, sıvıların ve katıların davranışını anlamada hayati bir rol oynar. Bu yazıda, kimyada yaygın olarak kullanılan basınç birimleri ve dönüşüm oranları ele alınarak, bu birimlerin uygulama alanları ve önemi vurgulanacaktır.
Kimyada Basınç Birimleri Nelerdir ve Nasıl Kullanılır?Kimyada basınç, birim alana uygulanan kuvvet olarak tanımlanır ve gazların, sıvıların ve katıların davranışını anlamada kritik bir rol oynar. Basınç birimleri, fiziksel sistemlerin analizinde kullanılan temel parametrelerdir. Bu makalede, kimyada yaygın olarak kullanılan basınç birimlerini ve bunların nasıl kullanıldığını ele alacağız. 1. Basınç BirimleriKimyada en yaygın basınç birimleri şunlardır:
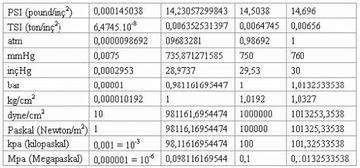
1.1 Pascal (Pa) Pascal, SI (Uluslararası Sistem) birimidir ve 1 Pa, 1 Newton'lık bir kuvvetin 1 m²'lik bir alana uygulanması durumunda oluşan basıncı ifade eder. Kimyasal reaksiyonların ve fiziksel değişimlerin incelenmesinde temel bir birim olarak kullanılır. 1.2 Atmosfer (atm)Atmosfer, deniz seviyesinde standart atmosfer basıncını ifade eden bir birimdir ve yaklaşık olarak 101325 Pa'ya eşittir. Genellikle gazların basınçlarını ifade etmek için kullanılır. 1.3 BarBar, basınç ölçümünde sıkça kullanılan bir başka birimdir ve 1 bar, 100000 Pa'ya eşittir. Genellikle endüstriyel uygulamalarda tercih edilir. 1.4 Milimetre Cıva (mmHg) Milimetre cıva, sıvıların basıncını ölçmek için yaygın olarak kullanılan bir birimdir. 1 mmHg, yaklaşık olarak 133.322 Pa'ya eşittir ve genellikle tıbbi ve bilimsel uygulamalarda kullanılır. 1.5 Tor (T)Tor, milimetre cıva ile aynı değere sahip bir basınç birimidir ve 1 Tor, 1 mmHg'ye eşittir. Genellikle vakum uygulamalarında kullanılır. 1.6 psi (pound per square inch)psi, özellikle Amerika Birleşik Devletleri'nde yaygın olarak kullanılan bir basınç birimidir. 1 psi, yaklaşık olarak 6894.76 Pa'ya eşittir ve genellikle otomotiv ve mühendislik alanlarında tercih edilir. 2. Basınç Birimlerinin Dönüşümü Farklı basınç birimleri arasında dönüşüm yapmak, kimyasal hesaplamalarda ve deneylerde oldukça önemlidir. Aşağıda bazı yaygın dönüşüm oranları verilmiştir:
Bu dönüşüm oranları, farklı basınç birimlerinin birbirine dönüştürülmesinde yardımcı olur ve deneysel verilerin karşılaştırılmasını kolaylaştırır. 3. Uygulama Alanları Basınç birimleri, çeşitli kimyasal ve fiziksel süreçlerde önemli bir rol oynar. Örneğin:
Bu uygulamalar, basınç ölçümlerinin ve birimlerinin doğru bir şekilde kullanılması gerektiğini vurgular. 4. Sonuç Kimyada basınç birimleri, gazların, sıvıların ve katıların davranışlarını anlamak için kritik öneme sahiptir. Çeşitli basınç birimlerinin doğru kullanımı ve dönüştürülmesi, deneysel verilerin güvenilirliğini artırır ve bilimsel çalışmalarda daha doğru sonuçlar elde edilmesini sağlar. Basınç birimlerinin önemini anlamak, kimya alanında başarılı bir kariyer için temel bir adımdır. Ekstra Bilgiler |


















Kimyada basınç birimleri konusunda verdiğin bilgiler gerçekten kapsamlı. Özellikle farklı birimlerin tanımları ve kullanım alanları çok faydalı. Pascal ve atmosfer gibi birimlerin, gazların davranışını anlamada nasıl kritik rol oynadığını düşündüğümde, laboratuvar deneylerinde bu birimlerin nasıl kullanıldığını merak ediyorum. Örneğin, bir gazın ideal gaz yasasına göre davranışını belirlemek için bu basınç birimlerinden hangisi daha yaygın kullanılıyor? Ayrıca, dönüşüm oranları hakkında daha fazla bilgi verirsen, deneysel verileri karşılaştırmada daha etkili olabilirim. Bu konudaki deneyimlerin neler?
Sayrak,
Laboratuvar Deneylerinde Basınç Birimleri
Laboratuvar deneylerinde, basınç birimleri konusunda genellikle pascal (Pa) ve atmosfer (atm) kullanılır. Pascal, SI birim sisteminde temel birimlerden biridir ve özellikle hassas ölçümlerin yapıldığı deneylerde tercih edilir. Atmosfer birimi ise gazların davranışlarını anlamak için daha yaygın bir referans noktası sağlar. Örneğin, ideal gaz yasası P = nRT formülünde basınç (P) genellikle atmosfer cinsinden ifade edilir, çünkü bu, gazların standart koşullar altında nasıl davrandığını gösteren pratik bir ölçümdür.
İdeal Gaz Yasası ve Basınç Birimleri
İdeal gaz yasasıyla çalışırken, çoğunlukla atmosfer birimi daha yaygın olarak kullanılır. Bunun nedeni, atmosferin gazların standart koşullar altında (0°C ve 1 atm) davranışlarını anlamak için yaygın bir referans olmasıdır. Ancak, daha hassas deneylerde pascal birimi tercih edilebilir. Özellikle laboratuvar ortamında, gazların davranışlarını incelemek için birim dönüşümleri yapmak önemlidir. Örneğin, 1 atm, yaklaşık 101325 Pa’ya eşittir. Bu dönüşüm oranını bilmek, deneysel verileri karşılaştırırken büyük kolaylık sağlar.
Dönüşüm Oranları
Dönüşüm oranları konusunda, 1 atm = 101.3 kPa, 1 atm = 760 mmHg ve 1 atm = 14.7 psi gibi oranlar oldukça önemlidir. Bu oranlar, farklı basınç birimleri arasında geçiş yaparken yardımcı olur ve deneysel verilerinizi karşılaştırma sürecinde oldukça etkili olabilir. Bu oranları bilmek, laboratuvar ortamında daha doğru ve tutarlı sonuçlar elde etmenizi sağlar.
Sonuç olarak, laboratuvar deneylerinde basınç birimlerinin doğru kullanımı, gazların davranışlarını anlamada kritik bir rol oynamaktadır. Bu konudaki deneyimlerinizi arttırmak için bu dönüşüm oranlarını ve birimlerin kullanımıyla ilgili bilgileri pratikte uygulamanız faydalı olacaktır.