
Gaz basıncı birimi nedir ve hangi birimler kullanılır?
Gaz basıncı, gazların moleküllerinin hareketiyle oluşturduğu birim alana uygulanan kuvveti ifade eder. Farklı birimlerde ölçülen gaz basıncı, fiziksel özellikler ve uygulama alanlarına göre değişiklik gösterir. Bu ölçümler, gazların davranışını ve çeşitli uygulamalardaki etkilerini anlamak açısından kritik öneme sahiptir.
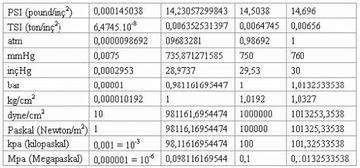
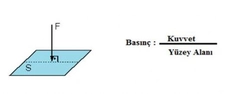
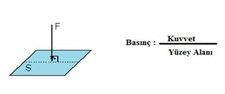
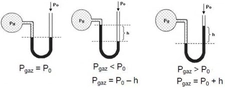
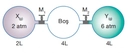
Gaz Basıncı Birimi Nedir?Gaz basıncı, bir gazın birim alana uyguladığı kuvvet olarak tanımlanır. Gazlar, moleküllerinin sürekli hareket etmesi nedeniyle, bulundukları kabın iç yüzeyine çarparak bir basınç oluştururlar. Bu basınç, gazın sıcaklığı, hacmi ve molekül sayısı gibi fiziksel özellikleriyle yakından ilişkilidir. Basınç, genellikle Pascal (Pa) cinsinden ölçülür, ancak farklı alanlarda farklı birimlerin kullanıldığı da görülmektedir. Gaz Basıncı Ölçüm BirimleriGaz basıncı ölçümünde kullanılan başlıca birimler şunlardır:
Pascal (Pa) Pascal, SI birim sisteminde basınç birimi olarak tanımlanmıştır. 1 Pascal, bir metrekarelik alana 1 Newton'luk bir kuvvetin uygulanması sonucu oluşan basıncı ifade eder. Gaz basıncını ölçmek için en yaygın kullanılan birimlerden biridir ve genellikle laboratuvar ölçümlerinde tercih edilir. BarBar, atmosfer basıncına yakın bir ölçü birimidir. 1 Bar, 100,000 Pascal'a eşittir. Genellikle sanayi uygulamalarında, özellikle hidrolik ve pnömatik sistemlerde kullanılır. Atmosfer (atm) Atmosfer, deniz seviyesinde bulunan ortalama hava basıncını ifade eder ve yaklaşık 101,325 Pascal'a eşittir. Bu birim, meteoroloji ve hava durumu raporlarında sıkça kullanılır. Milimetre Cıva (mmHg)Milimetre cıva, özellikle tıbbi uygulamalarda, örneğin kan basıncı ölçümlerinde yaygın olarak kullanılır. 1 mmHg, yaklaşık 133.322 Pascal'a eşittir. Bu birim, sıvıların basıncını ölçmek için sıklıkla tercih edilir. İnch Cıva (inHg)İnch cıva, özellikle hava basıncı ölçümünde kullanılır ve 1 inHg, yaklaşık 3,386 Pascal'a eşittir. Genellikle hava durumu raporlarında ve bazı endüstriyel uygulamalarda kullanılır. Torr Torr, 1 mmHg ile eşdeğer bir basınç birimidir. Özellikle vakum sistemlerinde ve analitik kimyada kullanılır. 1 Torr, yaklaşık 133.322 Pascal'a eşittir. Sonuç Gaz basıncı, çeşitli endüstriyel ve bilimsel uygulamalarda önemli bir parametre olup, farklı birimlerde ölçülmektedir. Bu birimler, gazın fiziksel özellikleri ve uygulama alanına göre değişkenlik gösterir. Basınç ölçümleri, gazların davranışını anlamak ve kontrol etmek için kritik öneme sahiptir. Ekstra Bilgiler Gaz basıncı ile ilgili olarak, ideal gaz yasası (PV=nRT) önemli bir kavramdır. Bu yasa, bir gazın basıncı (P), hacmi (V), mol sayısı (n), sıcaklık (T) ve gaz sabiti (R) arasındaki ilişkiyi tanımlar. Gazların davranışını anlamak için bu yasa sıkça kullanılır. Ayrıca, gaz basıncı, atmosferik basınç, iç basınç ve dış basınç gibi kavramlarla da ilişkilidir ve bu kavramların birbirleriyle etkileşimi, birçok fiziksel olayı etkileyebilir. |


















Gaz basıncı birimi hakkında bilgilendirici bir içerik okudum. Gazların moleküllerinin sürekli hareket etmesi nedeniyle belirli bir alana uyguladığı kuvvetin basıncı oluşturduğunu öğrenmek ilginçti. Farklı ölçüm birimlerinin, örneğin Pascal, Bar, atmosfer gibi, çeşitli alanlarda nasıl kullanıldığını görmek de oldukça faydalıydı. Pascal'ın SI birim sistemindeki önemi ve genellikle laboratuvarlarda tercih edildiği bilgilendirici bir detaydı. Özellikle atmosfer basıncının 101,325 Pascal olarak tanımlanması, hava durumu raporlarında neden bu birimin sıkça kullanıldığını anlamama yardımcı oldu. Gaz basıncının, ideal gaz yasası ile ilişkisini öğrenmek de gazların davranışını anlamak açısından önemli bir kavram. Diğer yandan, milimetre cıva ve inch cıva gibi birimlerin tıbbi uygulamalarda yaygın olarak kullanılması dikkatimi çekti. Gazların fiziksel özellikleri ve uygulama alanlarına göre değişkenlik gösteren basınç ölçümlerinin, endüstriyel ve bilimsel araştırmalardaki kritik rolü gerçekten ilgi çekici.
Pesin,
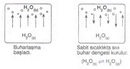
Gaz Basıncı ve Moleküllerin Hareketi hakkında öğrendiklerin gerçekten ilginç. Gazların moleküllerinin sürekli hareket etmesi ve belirli bir alana uyguladığı kuvvetin basıncı oluşturması, gazların davranışlarını anlamada temel bir kavram. Bu hareket, gazların genişleme ve sıkışma gibi özelliklerini de etkiliyor.
Farklı Ölçüm Birimleri konusuna değinmen de oldukça önemli. Pascal, Bar ve atmosfer gibi birimlerin farklı alanlarda kullanılması, gaz basıncının ölçülmesinde esneklik sağlıyor. Pascal'ın özellikle laboratuvarlarda tercih edilmesi, kesin ölçümler yapabilmek için önemli bir avantaj sunuyor.
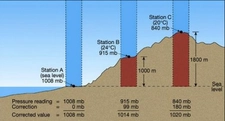
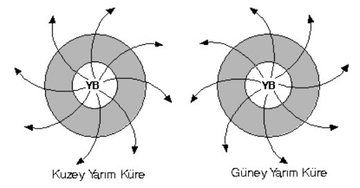
Atmosfer Basıncının Tanımı konusunda 101,325 Pascal'ın önemi, hava durumu raporlarında sıkça kullanılmasının nedenini açıklıyor. Bu bilgi, hava olaylarını anlamamızda bize yardımcı oluyor. Ayrıca, ideal gaz yasası ile gaz basıncı arasındaki ilişki, gazların sıcaklık ve hacimle nasıl etkileştiğini kavramak açısından kritik.
Tıbbi Uygulamalardaki Kullanım da dikkat çekici. Milimetre cıva ve inch cıva gibi birimlerin sağlık alanında yaygın kullanımı, basınç ölçümlerinin tıbbi teşhis ve tedavi süreçlerinde ne kadar önemli olduğunu gösteriyor.
Sonuç olarak, gaz basıncıyla ilgili öğrendiklerin, hem günlük hayatta hem de bilimsel çalışmalar açısından oldukça değerli bilgiler. Bu konudaki ilginin devam etmesi, gazların fiziksel özelliklerini ve uygulama alanlarını daha iyi anlamana yardımcı olacaktır.