
Basınç ve hacim ilişkisini açıklayan formül nedir?
Bu içerik, basınç ve hacim arasındaki ilişkiyi açıklayan temel fiziksel yasaları ele alıyor. Boyle Yasası ve ideal gaz yasası gibi formüller, gazların davranışını anlamak için kritik öneme sahip. Ayrıca, bu kavramların mühendislik ve bilim alanlarındaki uygulamalarını da vurguluyor.
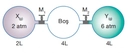
Basınç ve Hacim İlişkisini Açıklayan Formül Basınç ve hacim arasındaki ilişki, fizik ve mühendislik alanında önemli bir konudur. Bu ilişki, genellikle gazların davranışını anlamak için kullanılır ve temel olarak gazların durum denklemleri ile ifade edilir. Özellikle, Boyle Yasası bu ilişkiyi açıklayan en bilinen yasadır. Boyle Yasası Boyle Yasası, sabit bir sıcaklık altında bir gazın hacmi ile basıncı arasındaki ters orantıyı ifade eder. Yasaya göre, bir gazın basıncı (P) ile hacmi (V) arasındaki ilişki şu şekilde ifade edilir:
Bu ilişki, bir gazın hacmi azaldığında, basıncının arttığını ve hacmi arttığında, basıncının azaldığını göstermektedir. Bu durum, gaz moleküllerinin birbirine daha yakın olmasından kaynaklanır; bu da çarpışma sayısını artırarak basıncı yükseltir. Gazların Durum Denklemi Gazların davranışlarının daha kapsamlı bir analizi için, ideal gaz yasası kullanılabilir. Ideal gaz yasası şu şekilde ifade edilir:
Bu denklem, gazların davranışını açıklamak için hacim, basınç, sıcaklık ve madde miktarının nasıl etkileşimde bulunduğunu gösterir. Uygulama Alanları Basınç ve hacim ilişkisini açıklayan bu formüller, birçok alanda uygulanmaktadır. Bunlar arasında:
Bu uygulamalar, basınç ve hacim arasındaki ilişkiyi anlamanın önemini vurgulamaktadır. Sonuç Sonuç olarak, basınç ve hacim arasındaki ilişki, fiziksel olayların temelini oluşturan önemli bir konudur. Boyle Yasası ve ideal gaz yasası gibi formüller, bu ilişkiyi anlamak için kritik öneme sahiptir. Gazların davranışını anlamak, hem teorik hem de pratik uygulamalar açısından geniş bir yelpazede önem taşımaktadır. Bu bağlamda, basınç ve hacim ilişkisinin incelenmesi, bilim ve mühendislik disiplinlerinde kritik bir rol oynamaktadır. |


















Bu yazıda basınç ve hacim arasındaki ilişkiyi açıkça görmek mümkün. Boyle Yasası'nın gazların davranışını nasıl etkilediği ve bu ilişkinin pratikteki uygulamaları hakkında ne düşünüyorsunuz? Özellikle otomotiv mühendisliği veya tıp gibi alanlarda bu bilgilerin nasıl kullanıldığını gözlemlemek ilginç değil mi? Gazların hacminin azaldığında basıncının arttığını düşündüğümüzde, bu durumun gerçek hayattaki örnekleri neler olabilir?
Sinem,
Boyle Yasası ve Gazlar
Boyle Yasası, sabit sıcaklıkta bir gazın hacmi ile basıncı arasındaki ters orantıyı tanımlar. Yani, bir gazın hacmi azaldığında basıncı artar. Bu ilişki, gazların davranışını anlamak için oldukça kritik bir öneme sahiptir.
Pratik Uygulamalar
Otomotiv mühendisliği ve tıp gibi alanlarda, Boyle Yasası'nın uygulamaları oldukça yaygındır. Örneğin, otomotiv mühendisliğinde, motorların çalışma prensiplerini anlamak için bu yasa kullanılır. Motor silindirlerinde, hava ve yakıt karışımının basıncı, motorun verimliliğini doğrudan etkiler.
Tıp alanında ise, anestezi uygulamalarında gazların solunumu ve basıncı, hastaların güvenli bir şekilde anestetik gazları almasını sağlamak için kritik öneme sahiptir. Ayrıca, birçok tıbbi cihaz, gazların hacim ve basınç ilişkisini kullanarak çalışır.
Gerçek Hayattaki Örnekler
Gerçek hayatta, balonun üzerine bastırdığınızda hacminin azaldığını ve içindeki havanın basıncının arttığını gözlemleyebilirsiniz. Ayrıca, dağcılık gibi yüksek irtifalarda, basıncın azalması nedeniyle gazların genişlemesi ve bunun sonucunda hava kabarcıklarının oluşması gibi durumlar da gözlemlenir.
Sonuç olarak, Boyle Yasası'nın gazlar üzerindeki etkisi, birçok alanda pratik uygulamalarla kendini göstermekte ve gerçek hayatta karşılaştığımız birçok durumu açıklamamıza yardımcı olmaktadır. Bu bilgiler, mühendislik ve tıp gibi kritik alanlarda hayati önem taşımaktadır.