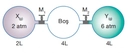
Basınç ve hacim arasında doğru orantı var mıdır?
Basınç ve hacim arasındaki ilişki, gazların davranışını anlamada temel bir rol oynamaktadır. Bu ilişki, fizik ve kimya alanlarında önemli bir yere sahiptir. Gazların basıncı, hacmi ve sıcaklığı arasındaki etkileşimler, çeşitli fiziksel olayları etkiler. Bu çalışma, bu ilişkiyi açıklayan temel yasaları incelemektedir.
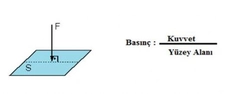
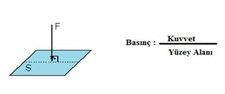
Basınç ve hacim arasındaki ilişki, gazların davranışlarını anlamak için temel bir konudur. Bu ilişki, özellikle fizik ve kimya alanında önemli bir yer tutar. Gazların basıncı, hacmi ve sıcaklığı arasındaki etkileşimler, birçok fiziksel olayı ve süreci etkiler. Bu makalede, basınç ve hacim arasındaki doğru orantı ilişkisi, ilgili fiziksel yasalar çerçevesinde incelenecektir. Basınç ve Hacim Kavramları Basınç, bir yüzeye uygulanan kuvvetin, yüzeyin alanına oranı olarak tanımlanır. Matematiksel olarak basınç, P = F/A formülü ile ifade edilir; burada P basıncı, F kuvveti ve A yüzey alanını temsil eder. Hacim ise bir nesnenin kapladığı üç boyutlu alanı ifade eder. Gazlar için hacim, genellikle litre veya metreküp cinsinden ölçülür. Gazların hacmi, sıcaklık ve basınç gibi dış etkenlere bağlı olarak değişkenlik gösterir. Ideal Gaz Yasası Basınç ve hacim arasındaki ilişkiyi anlamak için Ideal Gaz Yasası önemli bir referans noktasıdır. Ideal Gaz Yasası, bir gazın basıncı (P), hacmi (V) ve sıcaklığı (T) arasındaki ilişkiyi gösterir:
Burada n gazın mol sayısını, R ise ideal gaz sabitini temsil eder. Bu denklem, gazların davranışlarını öngörmek için kullanılır. Özellikle, belirli bir sıcaklıkta gazın basıncı ile hacmi arasında ters orantılı bir ilişki olduğu görülmektedir. Boyle Yasası Boyle Yasası, sabit sıcaklıkta bir gazın basıncı ile hacmi arasındaki ilişkiyi tanımlar. Bu yasa, gazların basıncı ile hacmi arasında ters orantılı bir ilişki olduğunu ifade eder:
Bu denklem, gazın hacmi arttıkça basıncın azaldığını, hacmi azaldıkça basıncın arttığını gösterir. Dolayısıyla, basınç ve hacim arasında doğru orantı yoktur; aksine, bu iki değişken arasında ters bir ilişki bulunmaktadır. Gazların Davranışı Gazların davranışını etkileyen çeşitli faktörler vardır. Bu faktörler arasında sıcaklık, moleküler yapı ve dış ortam koşulları bulunur. Basınç ve hacim arasındaki ilişki, bu faktörlerin etkisi altında değişebilir. Örneğin:
Sonuç Basınç ve hacim arasındaki ilişki, gazların davranışlarını anlamak için kritik bir öneme sahiptir. Boyle Yasası ve Ideal Gaz Yasası, bu ilişkiyi anlamamıza yardımcı olan temel prensiplerdir. Yine de, bu iki değişken arasında doğru orantı değil, ters orantı olduğu sonucuna varılmaktadır. Gazların davranışını etkileyen birçok faktör, basınç ve hacim arasındaki ilişkiyi karmaşık hale getirebilir. Ancak genel olarak, belirli koşullar altında gazların basıncının hacimle ters orantılı olduğu söylenebilir. Ekstra Bilgiler |