Basınç ve hacim nasıl ilişkilidir? (boyle yasası nedir?)
Bu içerik, basınç ve hacim arasındaki ilişkiyi açıklayan Boyle Yasası'nı detaylı bir şekilde ele alıyor. Boyle Yasası'nın tanımı, uygulama alanları ve sınırları üzerinde durulurken, gazların fiziksel özelliklerini anlamak için bu yasa ile birlikte diğer yasaların da önemine vurgu yapılıyor.
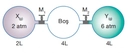
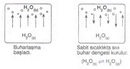
Basınç ve Hacim Nasıl İlişkilidir? (Boyle Yasası Nedir?)Basınç ve hacim arasındaki ilişki, fiziksel bilimlerin temel prensiplerinden biri olan Boyle Yasası ile açıklanır. Bu yasa, sabit sıcaklık altında bir gazın hacminin, basıncı ile ters orantılı olduğunu belirtir. Yani, bir gazın hacmi arttıkça, aynı sıcaklıkta basıncı azalır ve tam tersi durum da geçerlidir. Boyle Yasası ve Tanımı Boyle Yasası, 1662 yılında Robert Boyle tarafından formüle edilmiştir. Bu yasa, aşağıdaki matematiksel ifade ile özetlenebilir: P1 V1 = P2 V2 Burada:- P1 ve P2, gazın başlangıç ve son basınçlarını,- V1 ve V2 ise gazın başlangıç ve son hacimlerini temsil eder. Bu formül, sabit sıcaklık koşullarında gazın basıncı ile hacmi arasındaki ters orantıyı açıkça göstermektedir. Boyle Yasası'nın Uygulama Alanları Boyle Yasası, birçok bilimsel ve mühendislik alanında önemli bir rol oynamaktadır. Aşağıda bazı uygulama alanları sıralanmıştır:
Boyle Yasası'nın Sınırları Boyle Yasası, belirli koşullar altında geçerlidir. Bu koşullar şunlardır:
Gerçek gazlar, özellikle yüksek basınç ve düşük sıcaklık gibi koşullarda, ideal gaz davranışından sapabilir. Bu nedenle, Boyle Yasası'nın uygulanabilirliği, gazların gerçek koşullardaki davranışlarını anlamak için dikkatle ele alınmalıdır. Sonuç Sonuç olarak, basınç ve hacim arasındaki ilişki, Boyle Yasası ile açıkça tanımlanmıştır. Bu yasa, gazların fiziksel özelliklerini anlamak ve çeşitli uygulamalar geliştirmek için kritik bir öneme sahiptir. Yapılan deneyler ve gözlemler, gazların davranışlarını daha iyi anlamamıza ve mühendislik uygulamalarında daha verimli sistemler tasarlamamıza olanak tanımaktadır. Ekstra Bilgiler Boyle Yasası'nın yanı sıra, gazların davranışlarını açıklamak için başka yasalar da bulunmaktadır. Örneğin, Charles Yasası, gazların hacminin sıcaklık ile nasıl değiştiğini açıklar ve Avogadro Yasası, gazların hacminin molekül sayısı ile ilişkisini belirtir. Bu yasalar, gazların birbirleriyle etkileşimlerini anlamak için bir bütünlük oluşturur. Ayrıca, gazların davranışlarını inceleyen kinetik teori de, moleküler düzeyde gazların hareketlerini ve etkileşimlerini analiz eder. Bu nedenle, basınç, hacim ve sıcaklık arasındaki ilişkileri anlamak için bu yasaların bir arada değerlendirilmesi önemlidir. |